酮醇缩合反应
本文最后更新于:2020年5月18日 上午
文献和图片来源:Strategic Applications of Named Reactions in Organic Synthesis. Elsevier Academic Press。
本文仅供学习交流,如有侵权,请联系作者删除。
本文首发于B站专栏文章酮醇缩合反应。
要点
脂肪酯和熔融且高度分散于热二甲苯的金属钠反应,制备酮醇(α-羟基酮)的方法称为酮醇缩合反应。得到的酮醇二钠衍生物经酸化后释放出相应的酮醇。该类化合物是有价值的合成中间体。脂肪单酯生成对称化合物,而脂肪二酯生成环状酮醇。分子内酮醇缩合反应是制备10元闭环或更大闭环(最大可制备34元环)最好的方法之一。至于芳香酮醇(R为芳香取代基)的制备,采用两个芳香醛之间的安息香缩合反应即可。由于酮醇及酮醇负离子易于被氧化,因此酮醇缩合反应须在惰性气体中进行。加入TMSCl和使用超声使得合成小环酮醇(环尺寸:4-6)的收率大大提高。TMSCl的加入阻碍了碱催化的副反应,如:β-消除、Claisen缩合和Dieckmann缩合等,从而增加酮醇缩合反应的范围。得到的双硅氧烯烃或被直接分离,或经简单水解、醇解转化为酮醇化合物。
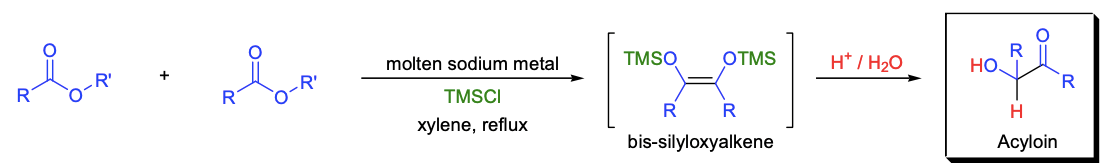
机理
对于酮醇缩合反应,现存有两种可能的机理。在机理A中,钠与酯通过单电子转移(SET)过程生成自由基负离子。该自由基负离子可二聚为二烷氧基双负离子。消除两个烷氧基负离子可得到二酮化合物。进一步的还原(电子从金属钠转移到二酮上)可生成新的双负离子,在酸性条件下后处理生成烯二醇,经互变异构得到酮醇化合物。机理B则提出了环氧中间体。
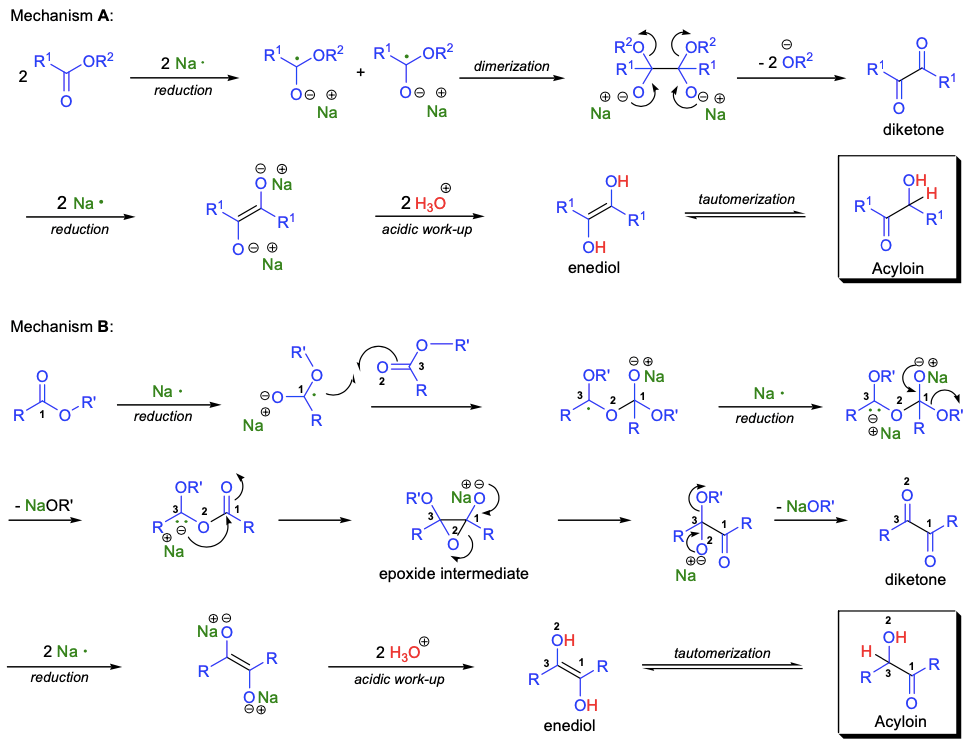
合成应用
J. Salaün和合作者研究了超声促进的酮醇缩合反应和羧酸酯的环化反应。他们发现1,4-、1,5和1,6-二酯的酮醇偶联可制备四、五、六元环产物。在TMSCl的存在下,β-氯酯经环化生成三元环产物。该反应需提前将金属钠高度分散于溶剂中。此外,在声化学的活化下,该反应得到了简化和改善。
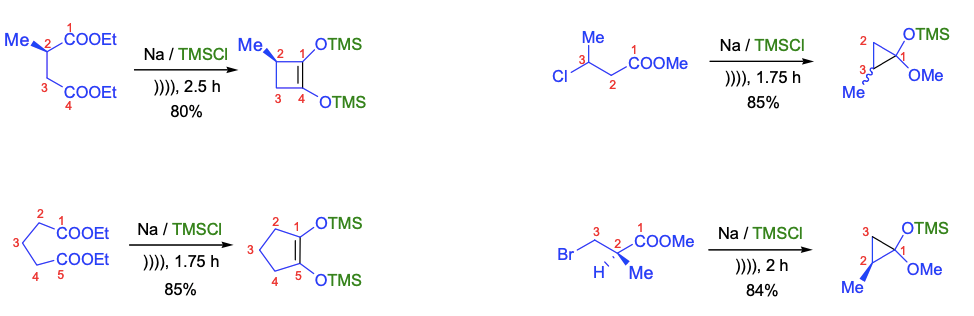
以Anopterine(R为巴豆酰基,即(E)-2,3-二甲基烯丙酰基)为主要成分的Anopterus二萜类家族生物碱与高水平的抗肿瘤活性相关。这类生物碱均含有三环[3.3.21,4.0]葵烷亚结构。S. Sieburth等人将酮醇缩合作为简洁构建该三环骨架的关键步骤。
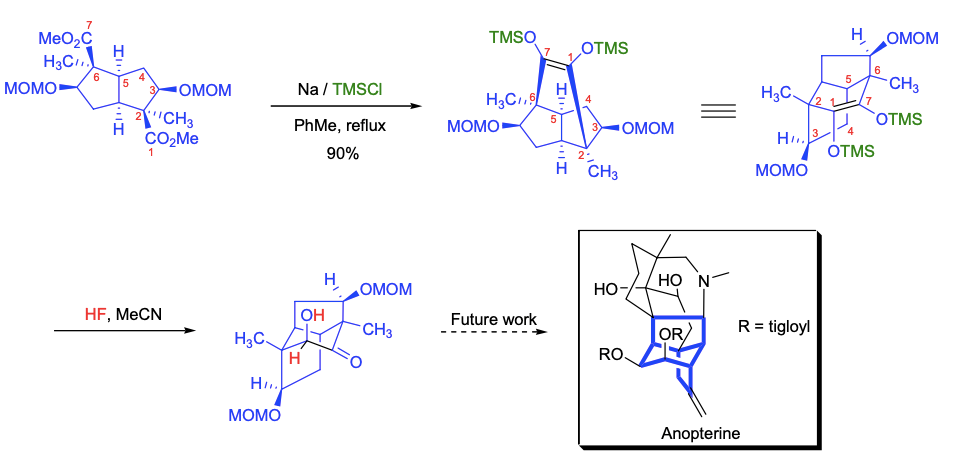
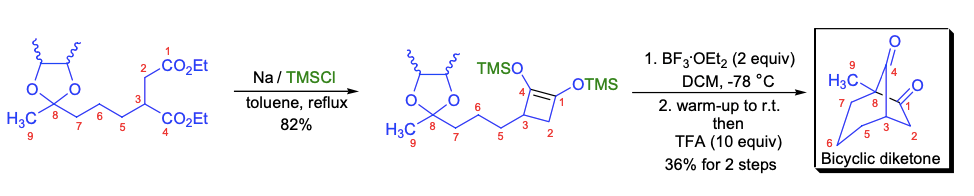
D. J. Burnell等人利用带缩酮侧链的环酮醇为前体,在Lewis酸的促进下,发生协同酰化反应合成双环二酮。所需的双硅氧烯烃用经典的酮醇缩合反应条件即可制备。
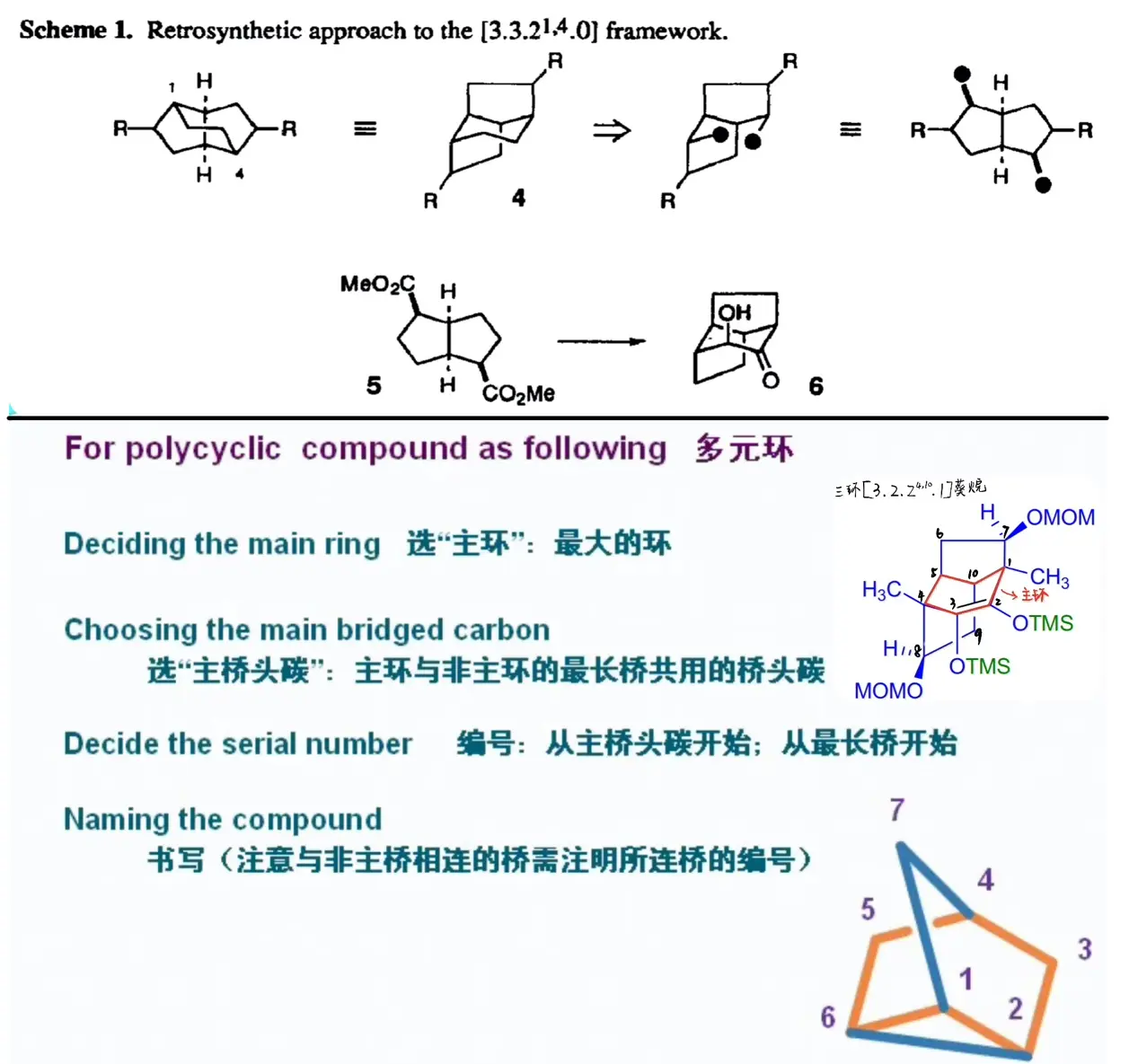
Pxxyyz有话要说:在第二个合成应用中,本书的作者直接采用了原文献[1]的命名方式,如下图。但是在书中又重新对化合物进行了编号。导致小P我在翻译过程中感觉食用效果不佳,因此又去看了李艳梅老师的《有机化学》公开课[2],结果我直接在风中凌乱,什么鬼??根据基础有机化学的命名规则,这个三环化合物可不能叫这个名字!!可能还有另外一套我所不知命名规则呢,世界之大,我等学艺不精,嘿嘿(求生欲)。。。小P我根据李老师课程中的命名三部曲试着给出了新的命名,三环[3.2.24,10.1]葵烷。如有错误,欢迎大家批评指正。
参考文献
[1] Hinman, M. M., Heathcock, C. H. A synthetic approach to the Stemona alkaloids. J. Org. Chem. 2001, 66, 7751-7756.
[2]《有机化学》刑奇毅;(李艳梅主讲《有机化学》)
本博客所有文章除特别声明外,均采用 CC BY-SA 4.0 协议 ,转载请注明出处!
